El Instituto de Investigación Hospital Universitario 12 de Octubre (i+12), en colaboración con la ONCE, está llevando a cabo un estudio consistente en la generación de un modelo humano in vitro de células ganglionares de la retina -RGCs- que será utilizado como plataforma para probar fármacos contra la atrofia óptica dominante -DOA-, una enfermedad rara, progresiva e irreversible que causa ceguera y una de las formas más frecuentes de neuropatía óptica hereditaria.
Este proyecto, llevado a cabo por la doctora María Esther Gallardo del Grupo de Investigación Traslacional con Células iPS del i+12, pretende generar modelos in vitro de RGCs paciente-específicas, empleando para ello una metodología de vanguardia basada en el uso de células madre pluripotentes inducidas (iPS). Estos modelos se desarrollarán para ser utilizados como plataforma para ensayar fármacos y compuestos con potencial actividad farmacológica, con el fin de evaluar posibles tratamientos para la DOA fácilmente transferibles a la práctica clínica, teniendo en cuenta el tipo de compuesto que será analizado.
El proyecto persigue que estos modelos también supongan un gran paso hacia adelante en el conocimiento de los mecanismos fisiopatológicos de la DOA, al ser investigados directamente en el tipo celular diana afectado en estos pacientes (RGCs), algo que no sería factible de otra forma, ya que las RGCs de los pacientes no son fácilmente accesibles salvo en los tejidos post-mortem.
Este proyecto entra dentro de lo que se conoce como medicina personalizada, ya que la previsión es que tenga un impacto directo en la calidad de vida de los pacientes y reduzcan los impactos socio-económicos y personales negativos de este tipo de enfermedades.
La DOA es una enfermedad mitocondrial de origen nuclear que conduce a una degeneración específica de las RGCs y que compromete la transmisión de la información visual de la retina al cerebro. Muchos pacientes con esta patología evolucionan hacia ceguera legal, sin existir actualmente tratamiento para este trastorno, debido en parte a la falta de un modelo adecuado con el que investigar. Por lo tanto, es muy relevante desarrollar nuevos sistemas experimentales, idealmente de origen humano, que permitan crear modelos sobre la DOA que puedan ser útiles como plataforma para la investigación de tratamientos.
Este estudio se está desarrollando gracias al programa Ayudas a la Investigación de la ONCE que apoya y estimula el conocimiento científico más avanzado e innovador en la prevención de la ceguera y el desarrollo de terapias efectivas para quienes tienen o pueden desarrollar problemas graves de visión.
FUENTE: Comunidad de Madrid





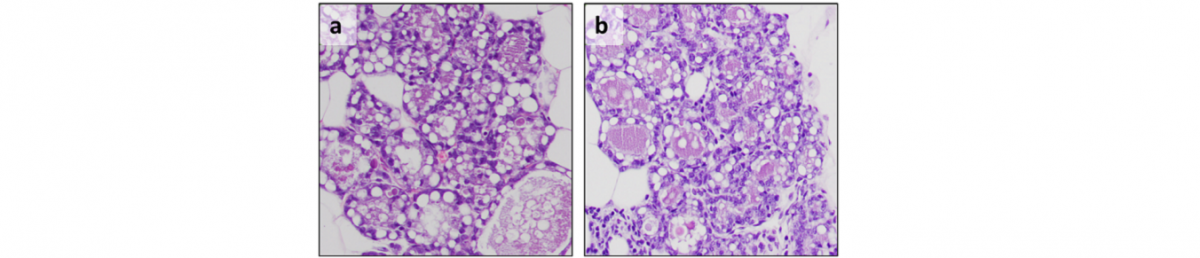
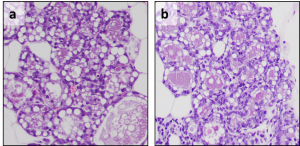 Figura: microfotografías de cortes histológicos de glándulas mamarias de hembras en el día 17,5 de gestación. (a) animal control; (b) animal con expresión de ERAS en células mioepiteliales. Obsérvese cómo las células mioepiteliales presentan nucleomegalia (mayor tamaño del núcleo) como consecuencia de la expresión de ERAS (flechas).
Figura: microfotografías de cortes histológicos de glándulas mamarias de hembras en el día 17,5 de gestación. (a) animal control; (b) animal con expresión de ERAS en células mioepiteliales. Obsérvese cómo las células mioepiteliales presentan nucleomegalia (mayor tamaño del núcleo) como consecuencia de la expresión de ERAS (flechas).